För omvandlingen av ljusfotoner till elektriska signaler i näthinnan krävs närvaro av det 65-kilodaltons protein som är specifikt för näthinnans pigmentepitel (RPE65). RPE65 finns i näthinnans pigmentepitelceller och konverterar all-trans-retinol till 11-cis-retinol som sedan bildar kromoforen 11-cis-retinal under syncykeln (retinoidcykeln).1
Mutationer av genen RPE65 leder till nedsatt eller obefintlig aktivitet av RPE65 all-trans-retinyl isomeras, vilket blockerar syncykeln och leder till synförlust. Med tiden ackumuleras toxiska ämnen vilket leder till att näthinnans pigmentepitelceller dör och därefter till progressiv fotoreceptorcelldöd.1
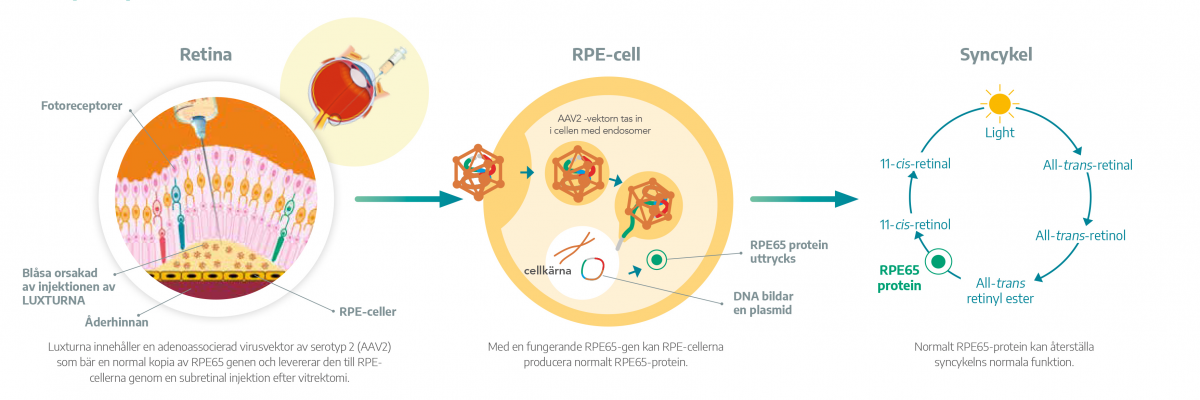
När Luxturna injiceras i det subretinala rummet, sker transduktion av näthinnans pigmentepitelceller med cDNA:t som kodar för normalt humant RPE65 protein (genaugmentationsterapi), vilket gör återställning av syncykeln möjlig.
Referenser
-
Luxturna® SPC

